2×Taq PCR MasterMix
Functies
■ Hoge amplificatie-efficiëntie: DNA-fragmenten van verschillende groottes (minder dan 5 kb) en bronnen kunnen efficiënt worden geamplificeerd.
■ Hoge gevoeligheid: slechts 10 pg doelfragmenten kunnen worden geamplificeerd uit genomische templates.
■ Hoge stressbestendigheid: voor sjablonen met een hoog gehalte aan onzuiverheden, zoals ruw geëxtraheerde sjabloon/bacteriecultuur, kan het doelfragment gemakkelijk worden geamplificeerd. De polymerase-activiteit wordt niet beïnvloed door herhaaldelijk invriezen en ontdooien.
■ Handig voor toepassingen: het reactiesysteem werd eenvoudig en snel voorbereid. Het geamplificeerde fragment bevat de 3'-uiteinde dA-overhang, wat handig is voor TA-klonering.
Specificatie
Type: Taq DNA-polymerase
Steekproef: Gezuiverd/ruw geëxtraheerd sjabloon/bacteriecultuur
Sjabloon: >10 pg
Fragmentgrootte: <5 kb
Toepassingen: PCR-amplificatie van DNA-fragmenten, DNA-labeling, primerverlenging, sequentiebepaling, grootschalige gendetectie, semi-kwantitatieve PCR-experimenten, detectie van sporen-DNA, enz.
Alle producten kunnen worden aangepast voor ODM/OEM. Voor details,klik op Aangepaste Service (ODM/OEM)
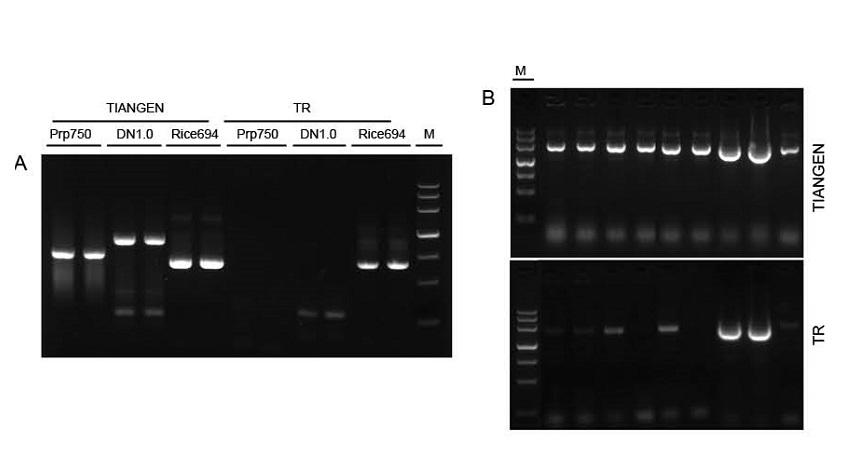 |
Figuur 1. Sjablonen uit verschillende bronnen werden geamplificeerd door respectievelijk TIANGEN Taq MasterMix II en de gewone Taq Mix van Supplier TR om de stressbestendigheid van de reagentia te detecteren. De resultaten laten zien dat TIANGEN-producten de doelfragmenten van ruwe genomische sjablonen en bacteriecultuur kunnen amplificeren, en dat de stressbestendigheid beter is dan die van leverancier TR. A: Ruwe genomische sjabloon geëxtraheerd door TIANGEN TIANcombi DNA Lyse & Det PCR Kit. Prp/DN: Ruwe extractie en detectie van menselijke bloedmonsters. Rijst: Ruwe extractie en detectie van rijstmonsters. B: Kolonie PCR. Het PCR-fragment is 700 bp. M: TIANGEN Marker III |
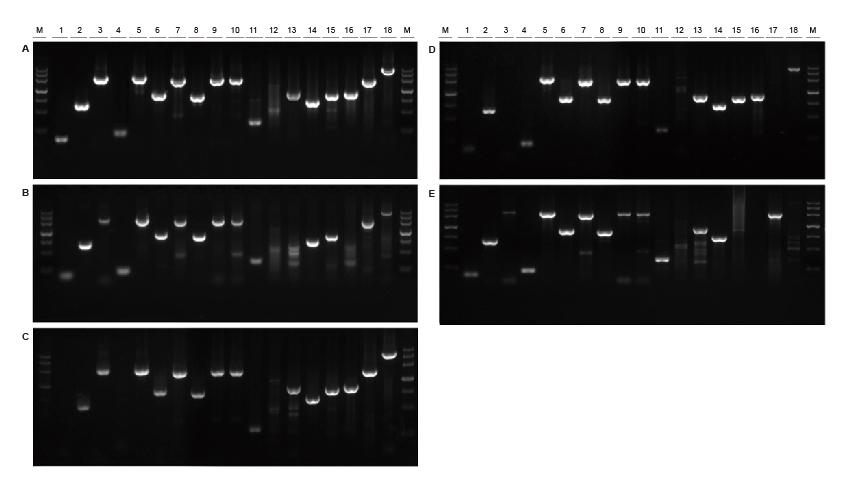 |
Goede universaliteit voor sjablonen uit verschillende bronnen en met verschillende lengtes Figuur 2. Fragmenten van verschillende bronnen en lengtes werden geamplificeerd met behulp van TIANGEN Taq MasterMix II (A) en gewoon Taq Mix van respectievelijk leverancier TK (B), leverancier TR (C), leverancier V (D) en leverancier G (E). De resultaten tonen aan dat de uitgebreide prestatie van TIANGEN-producten de beste is in termen van amplificatievermogen, specificiteit en universaliteit. M: TIANGEN Marker III1: Sojaboon genomisch DNA-template (120 bp); 2-3: Genomisch DNA-matrijs van rijst (694 bp, 2258 bp); 4: Katoen genomisch DNA-matrijs (200 bp); 5: Escherichia coli genomische DNA-matrijs (2298 bp); 6-7: Matrijs van muisgenoom-DNA (1 kb, 2 kb); 8-10: Rat genomisch DNA-matrijs (1 kb, 2 kb, 2080 bp); 11-18: Human genoom-DNA-template (300 bp, 448 bp (GC%: 74,8%), 1100 bp, 750 bp, 1000 bp, 1090 bp (GC%: 70,4%), 2 kb, 4 kb) |
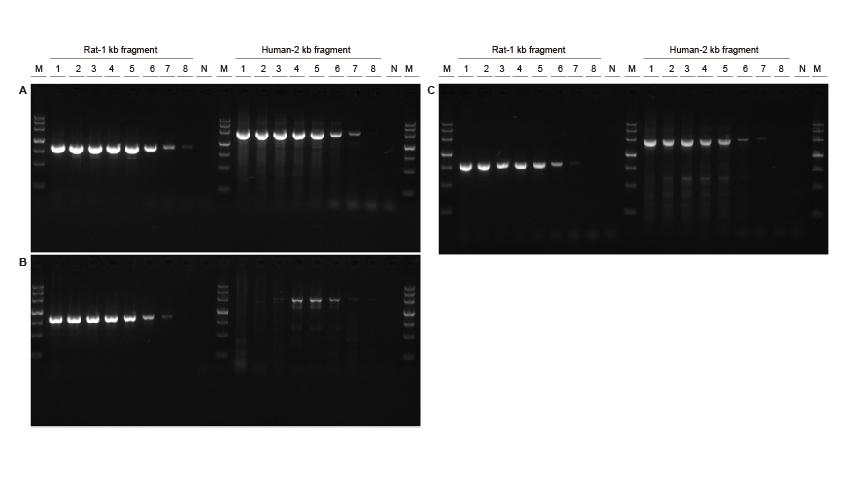 |
Hoge gevoeligheid Figuur 3. Verschillende concentraties van DNA-fragmenten van ratten en mensen werden geamplificeerd met behulp van TIANGEN Taq MasterMix II (A), gewoon Taq Mix van respectievelijk leverancier V (B) en leverancier TK (C), om de versterkingsgevoeligheid te detecteren. De resultaten laten zien dat het TIANGEN-product het doelfragment van de genoomsjabloon kan amplificeren tot slechts 0,01 ng, en de gevoeligheid ervan is beter dan die van de producten van leverancier V en TK.M: TIANGEN Marker III, N: NTCTemplate input 1-8 : 200 ng, 100 ng, 50 ng, 20 ng, 10 ng, 1 ng, 0,1 ng, 0,01 ng. |
A-1-sjabloon
■ De template bevat eiwitonzuiverheden of Taq-remmers, enz. ——Zuiver DNA-template, verwijder eiwitonzuiverheden of extraheer template-DNA met zuiveringskits.
■ De denaturatie van de mal is niet volledig ——Verhoog de denaturatietemperatuur op de juiste manier en verleng de denaturatietijd.
■ Sjabloondegradatie ——Maak de sjabloon opnieuw.
A-2 Primer
■ Slechte kwaliteit van primers ——Hersynthetiseer de primer.
■ Degradatie van de primer ——Verdeel de primers met een hoge concentratie in een klein volume voor conservering. Vermijd meerdere keren invriezen en ontdooien of langdurig 4°C gecryopreserveerd.
■ Onjuist ontwerp van primers (bijv. primerlengte niet voldoende, dimeer gevormd tussen primers, enz.) - Herontwerp primers (vermijd vorming van primerdimeer en secundaire structuur)
A-3 Mg2+concentratie
Mg2+ concentratie is te laag ——Verhoog Mg . op de juiste manier2+ concentratie: Optimaliseer de Mg2+ concentratie door een reeks reacties van 1 mM tot 3 mM met een interval van 0,5 mM om de optimale Mg . te bepalen2+ concentratie voor elke sjabloon en primer.
A-4 Onthardingstemperatuur
■ De hoge annealingstemperatuur beïnvloedt de binding van primer en template. ——Verlaag de gloeitemperatuur en optimaliseer de conditie met een gradiënt van 2°C.
A-5 Verlengingstijd
■ Korte verlengingstijd—Verhoog de verlengingstijd.
Fenomenen: Negatieve monsters tonen ook de doelsequentiebanden.
A-1 Contaminatie van PCR
■ Kruisbesmetting van doelsequentie of amplificatieproducten ——Pas het monster met de doelsequentie voorzichtig in het negatieve monster of mors ze niet uit de centrifugebuis. De reagentia of apparatuur moeten worden geautoclaveerd om bestaande nucleïnezuren te verwijderen, en het bestaan van verontreiniging moet worden bepaald door middel van negatieve controle-experimenten.
■ Reagensverontreiniging ——Verdeel de reagentia en bewaar ze bij lage temperatuur.
A-2 Primer
Mg2+ concentratie is te laag ——Verhoog Mg . op de juiste manier2+ concentratie: Optimaliseer de Mg2+ concentratie door een reeks reacties van 1 mM tot 3 mM met een interval van 0,5 mM om de optimale Mg . te bepalen2+ concentratie voor elke sjabloon en primer.
■ Onjuist primerontwerp en de doelsequentie heeft homologie met de niet-doelsequentie. ——Herontwerp inleidingen.
Verschijnselen: De PCR-amplificatiebanden zijn niet consistent met de verwachte grootte, groot of klein, of soms komen zowel specifieke amplificatiebanden als niet-specifieke amplificatiebanden voor.
A-1 Primer
■ Slechte primerspecificiteit
—— Herontwerp de inleiding.
■ De primerconcentratie is te hoog —— Verhoog de denaturatietemperatuur op de juiste manier en verleng de denaturatietijd.
A-2 Mg2+ concentratie
■ De Mg2+ concentratie is te hoog ——Verlaag de Mg2+-concentratie op de juiste manier: Optimaliseer de Mg2+ concentratie door een reeks reacties van 1 mM tot 3 mM met een interval van 0,5 mM om de optimale Mg . te bepalen2+ concentratie voor elke sjabloon en primer.
A-3 Thermostabiele polymerase
■ Overmatige hoeveelheid enzym ——Verminder de hoeveelheid enzym op geschikte wijze met tussenpozen van 0,5 E.
A-4 Onthardingstemperatuur
■ De gloeitemperatuur is te laag — Verhoog de gloeitemperatuur op de juiste manier of gebruik de gloeimethode in twee fasen
A-5 PCR-cycli
■ Te veel PCR-cycli ——Verminder het aantal PCR-cycli.
A-1 Primer——Slechte specificiteit ——Herontwerp de primer, verander de positie en lengte van de primer om de specificiteit te verbeteren; of voer geneste PCR uit.
A-2 Sjabloon-DNA
——De sjabloon is niet zuiver ——Zuiver de sjabloon of extraheer DNA met zuiveringskits.
A-3 Mg2+ concentratie
——Mg2+ concentratie is te hoog ——Mg . op de juiste manier verminderen2+ concentratie: Optimaliseer de Mg2+ concentratie door een reeks reacties van 1 mM tot 3 mM met een interval van 0,5 mM om de optimale Mg . te bepalen2+ concentratie voor elke sjabloon en primer.
A-4 dNTP
——De concentratie van dNTP's is te hoog ——Verlaag de concentratie van dNTP op de juiste manier
A-5 Onthardingstemperatuur
——Te lage gloeitemperatuur ——Verhoog de gloeitemperatuur op gepaste wijze
A-6 Cycli
——Te veel cycli ——Optimaliseer het cyclusnummer

De eerste stap is het kiezen van de juiste polymerase. Regulier Taq-polymerase kan niet proeflezen vanwege een gebrek aan 3'-5'-exonuclease-activiteit, en mismatch zal de verlengingsefficiëntie van fragmenten aanzienlijk verminderen. Daarom kan regulier Taq-polymerase doelfragmenten groter dan 5 kb niet effectief amplificeren. Taq-polymerase met speciale modificatie of andere high-fidelity-polymerase moet worden geselecteerd om de verlengingsefficiëntie te verbeteren en te voldoen aan de behoeften van amplificatie van lange fragmenten. Bovendien vereist de amplificatie van lange fragmenten ook een overeenkomstige aanpassing van het primerontwerp, denaturatietijd, verlengingstijd, buffer-pH, enz. Gewoonlijk kunnen primers met 18-24 bp tot een betere opbrengst leiden. Om schade aan de mal te voorkomen, moet de denaturatietijd bij 94°C worden teruggebracht tot 30 sec of minder per cyclus, en de tijd om de temperatuur te verhogen tot 94°C vóór amplificatie moet minder dan 1 minuut zijn. Bovendien kan het instellen van de verlengingstemperatuur op ongeveer 68°C en het ontwerpen van de verlengingstijd volgens de snelheid van 1 kb/min zorgen voor effectieve amplificatie van lange fragmenten.
Het foutenpercentage van PCR-amplificatie kan worden verminderd door verschillende DNA-polymerasen met hoge betrouwbaarheid te gebruiken. Van alle Taq-DNA-polymerasen die tot nu toe zijn gevonden, heeft het Pfu-enzym het laagste foutenpercentage en de hoogste betrouwbaarheid (zie bijgevoegde tabel). Naast enzymselectie kunnen onderzoekers de PCR-mutatiesnelheid verder verlagen door de reactieomstandigheden te optimaliseren, waaronder het optimaliseren van de buffersamenstelling, de concentratie van thermostabiel polymerase en het optimaliseren van het aantal PCR-cycli.
Producten categorieën
WAAROM VOOR ONS KIEZEN
Sinds de oprichting heeft onze fabriek eersteklas producten ontwikkeld volgens het principe:
van kwaliteit voorop. Onze producten hebben een uitstekende reputatie verworven in de industrie en zijn waardevol bij nieuwe en oude klanten.








